솔베이 공정
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
솔베이 공정은 탄산나트륨을 생산하는 화학 공정으로, 1860년대 벨기에의 에르네스트 솔베이에 의해 개발되었다. 이 공정은 암모니아를 이용한 브라인(소금물)에 이산화탄소를 통과시켜 중탄산나트륨을 침전시키고, 이를 소성하여 탄산나트륨을 얻는 방식으로 진행된다. 솔베이 공정은 르블랑 공정을 대체하며 19세기 말까지 세계 소다회 생산을 주도했으나, 20세기 초 트로나 광상의 발견과 수산화나트륨 생산 증가로 인해 쇠퇴했다. 솔베이 공정은 염화칼슘 폐기물과 이산화탄소 배출이라는 환경 문제를 야기하며, 이를 개선하기 위한 노력이 이루어지고 있다.
더 읽어볼만한 페이지
- 암모니아 - 암모니아수
암모니아수는 암모니아(NH3)가 물(H2O)에 용해된 수용액으로, 염기성을 띠며 세척제, 산업용, 식품 첨가물, 실험실 시약 등 다양한 용도로 사용된다. - 암모니아 - 고암모니아혈증
고암모니아혈증은 혈중 암모니아 수치가 정상 범위를 초과하는 상태로, 선천적 대사 이상이나 후천적 간 기능 부전 등으로 발생하며, 신경학적 문제, 발작, 뇌병증, 혼수 등을 유발하고 암모니아 생성 억제 및 배설 촉진 치료를 시행한다. - 화학공학 공정 - 디카페인
디카페인은 커피나 차에서 카페인을 제거한 제품을 의미하며, 유기 용매, 물, 초임계 이산화탄소 등을 이용한 탈카페인 기술로 제조되거나 카페인 없는 커피나무를 재배하는 방법으로 생산된다. - 화학공학 공정 - 건조
건조는 물질 속 수분을 증발시켜 고체나 반고체 상태로 만드는 과정으로, 식품 보존, 화학 실험, 산업 공정, 방송 공학, 생물학 연구 등 다양한 분야에서 활용되며 DNA 손상을 유발하거나 미생물의 저항성을 진화시키기도 한다.
| 솔베이 공정 | |
|---|---|
| 기본 정보 | |
 | |
| 다른 이름 | 암모니아-소다 공정 |
| 발견자 | 에르네스트 솔베이 |
| 발견 연도 | 1861년 |
| 관련 물질 | 탄산 나트륨 암모니아 이산화 탄소 염화 나트륨 탄산 칼슘 |
| 공정 개요 | |
| 원리 | 화학 평형 용해도 차이 이용 |
| 주요 단계 | 암모니아 포화된 소금물 제조 이산화 탄소 주입 중탄산 나트륨 침전 탄산 나트륨 생산 |
| 부산물 | 염화 칼슘 |
| 폐기물 처리 | 암모니아 회수 및 재사용 |
| 화학 반응식 | |
| 전체 반응 | 2 NaCl + CaCO3 → Na2CO3 + CaCl2 |
| 주요 반응 | NH3 + H2O + CO2 → NH4HCO3 NH4HCO3 + NaCl → NaHCO3 + NH4Cl 2 NaHCO3 → Na2CO3 + H2O + CO2 |
| 장점 | |
| 이점 | 비교적 저렴한 원료 사용 대량 생산 가능 암모니아 회수를 통해 효율성 증대 |
| 단점 | |
| 문제점 | 염화 칼슘 부산물 발생 에너지 소비량 많음 공정 과정에서 환경 오염 발생 가능성 |
| 역사 | |
| 배경 | 천연 탄산 나트륨 공급 부족 |
| 개발 동기 | 르블랑 공정의 단점 극복 탄산 나트륨의 대량 생산 필요 |
| 솔베이의 기여 | 공정 개선 및 산업화 성공 |
| 응용 분야 | |
| 활용 분야 | 유리 제조 세제 제조 화학 제품 생산 제지 공업 수처리 |
| 경제적 영향 | |
| 영향 | 탄산 나트륨 가격 하락 및 대중화 기여 |
| 관련 산업 발전 | 유리 산업 성장 세제 산업 성장 |
| 환경적 영향 | |
| 논란 | 염화 칼슘 폐기물 처리 문제 |
| 개선 노력 | 염화 칼슘 활용 방안 연구 에너지 효율 향상 노력 |
| 참고 문헌 | |
| 참고 문헌 | Oxford Reference - Solvay process 화학대사전 (화학대사전편집위원회 편, 共立, 1981) |
2. 역사
"소다회"라는 이름은 알칼리를 얻는 주요한 역사적 방법인 특정 식물의 재에서 물을 사용하여 알칼리를 추출하는 방법에서 유래했다. 나무 재는 초석회와 그 주요 성분인 탄산칼륨(K2CO3)을 생성했지만, 이러한 특수 식물의 재는 "소다회"와 그 주요 성분인 탄산나트륨(Na2CO3)을 생성했다. "소다"라는 단어(중세 라틴어에서 유래)는 원래 소금에 녹는 성분이 있는 특정 식물을 가리켰다. 이러한 식물의 재에서 유용한 알칼리인 소다회를 얻을 수 있다는 것이 발견되었다. 이러한 식물의 재배는 18세기 스페인에서 특히 발달했는데, 이 식물은 ''바릴라''(또는 영어로 "바릴라")라고 불린다.[3][4][5] 켈프의 재도 소다회를 생성하며, 18세기 스코틀랜드의 거대한 산업의 기반이 되었다.[6] 알칼리는 이집트의 건조한 호수 바닥에서도 채굴되었다.
1811년 프랑스 물리학자 오귀스탱 장 프레넬은 암모니아를 함유한 브라인에 이산화탄소를 통과시키면 중탄산나트륨이 침전된다는 것을 발견했지만, 이 발견은 발표되지 않았다. 데스몬드 레일리는 "암모니아-소다 공정의 발전 이야기는 발견이 이루어진 후 한동안 방치되고 적용되지 않는 방식의 흥미로운 사례"라고 지적했다.[8] 이 반응을 산업 공정의 기반으로 심각하게 고려한 것은 1834년 H. G. 다이어와 J. 헤밍에게 발행된 영국 특허부터이며, 이후 여러 차례 시도가 있었으나 성공 여부는 다양했다.
1884년, 솔베이 형제는 미국인 윌리엄 B. 코그스웰과 로랜드 해저드에게 미국에서 소다회를 생산할 수 있는 라이선스를 부여하고, 솔베이 공정 회사라는 합작 투자를 설립하여 뉴욕주 솔베이에 공장을 건설하고 운영했다.
2. 1. 르블랑 공정
18세기 말, 유럽에서 비누, 섬유, 유리 산업이 발전하면서 알칼리 수요가 급증했다.[7] 1791년, 프랑스 의사 니콜라 르블랑은 소금, 석회석, 황산, 석탄을 사용하여 소다회를 제조하는 방법을 개발했다. 르블랑 공정은 19세기 초 알칼리 생산을 지배하게 되었지만, 투입 재료의 비용과 염화수소 가스를 포함한 오염 부산물 때문에 이상적인 해결책과는 거리가 멀었다.[7][9]2. 2. 솔베이 공정의 등장
1861년, 벨기에의 산업 화학자 에르네스트 솔베이는 르블랑 공정의 문제점에 주목했다.[9] 그는 이전의 연구를 거의 알지 못했지만, 이산화탄소가 하강하는 브라인 흐름을 통해 거품이 되는 24m 가스 흡수탑을 개발하여 이 문제를 해결했다.[9] 이 흡수탑과 암모니아의 효율적인 회수 및 재활용을 통해 솔베이 공정은 르블랑 공정보다 더 경제적이고 오염이 적은 공정으로 입증되었다.1864년, 솔베이와 그의 형제 알프레드는 재정적 지원을 확보하여 샤를루아 근처 쿠이예에 첫 솔베이 공장을 건설했다. 1874년에는 낭시에 더 큰 공장을 건설하여 시설을 확장했다.
같은 해, 루트비히 몬드는 솔베이를 방문하여 새로운 기술 사용 권리를 획득했다. 그는 존 브루너와 함께 브루너 몬드 회사를 설립하고, 노스위치 근처 위닝턴에 솔베이 공장을 건설하여 1874년부터 가동을 시작했다. 몬드는 솔베이 공정의 상업적 성공에 중요한 역할을 했는데, 1873년부터 1880년 사이에 공정을 지연시키거나 중단시킬 수 있는 부산물을 제거하는 개선을 이루어냈다.
솔베이 공정은 르블랑 공정에 비해 생성물의 순도가 높고, 폐기물이 적으며, 저렴하게 생산할 수 있다는 장점 덕분에 빠르게 확산되었다.[25] 1890년대까지 솔베이 공정 공장은 세계 소다회의 대부분을 생산하게 되었다.
2. 3. 솔베이 공정의 확산과 쇠퇴
솔베이법은 르블랑법에 비해 생성물의 순도가 높고, 폐기물이 적으며 저렴하게 생산할 수 있어 상업적으로 우수했다. 1872년 영국에 솔베이법으로 탄산나트륨을 생산하는 공장이 건설된 이후, 솔베이법은 빠르게 전 세계로 확산되어 르블랑법을 대체하고 주류가 되었다.[25]1938년 미국에서 트로나의 대규모 천연 광상이 발견되면서 천연 탄산나트륨을 저렴하게 얻을 수 있게 되었다. 또한 염화비닐 등의 원료로 많은 염소가 필요한 현대에는, 식염수의 전기분해로 발생하는 수산화나트륨이 과잉 생산되기 때문에, 수산화나트륨을 이산화탄소로 중화시켜 제조하는 탄산나트륨의 양도 무시할 수 없을 정도로 많아졌다. 이러한 이유로 솔베이법은 상당히 쇠퇴했다.
3. 화학 반응
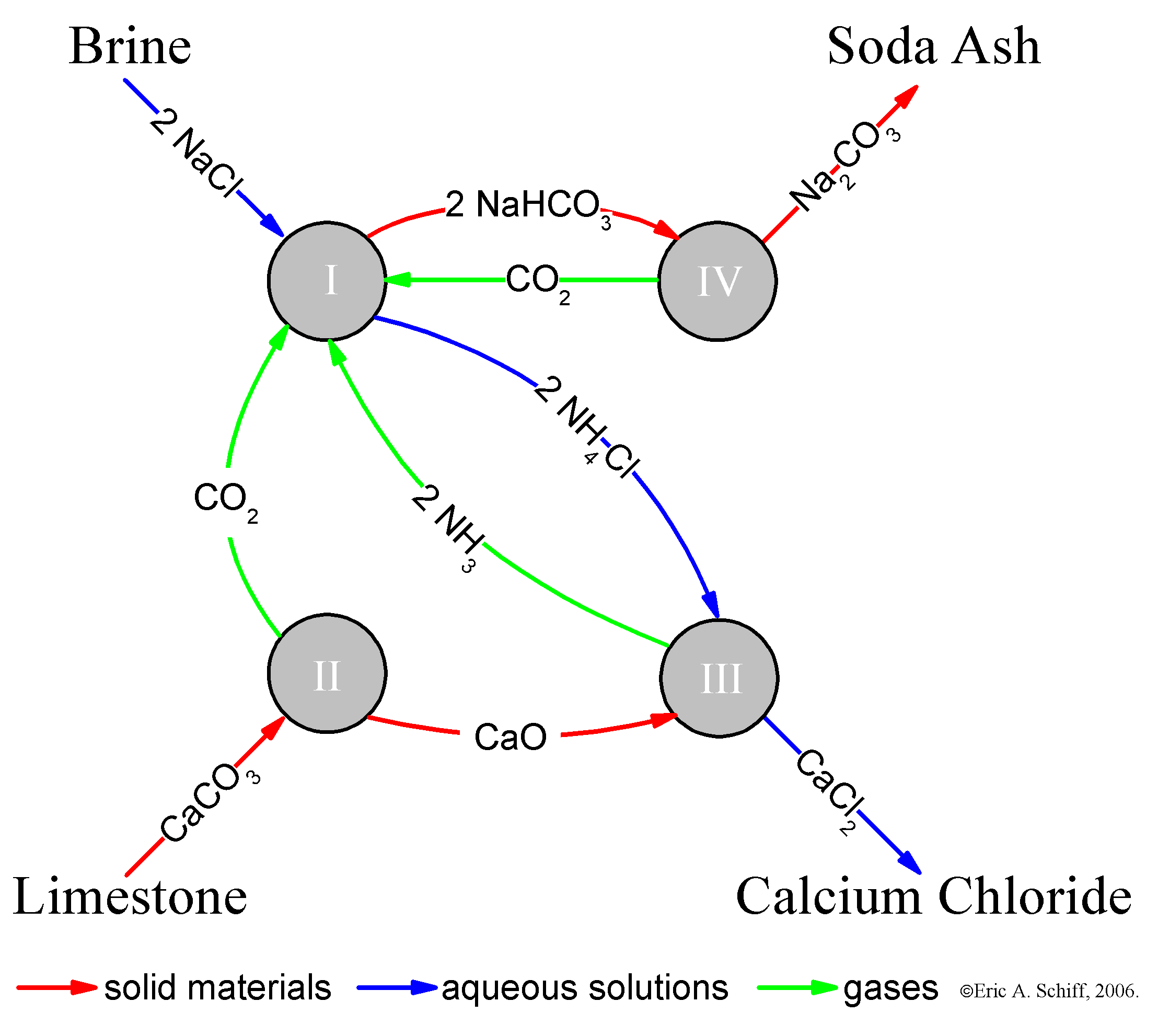
솔베이 공정은 탄산화 공정, 소성 공정, 암모니아 증류 공정의 세 단계로 이루어진다.[22] 각 공정에서 일어나는 화학 반응은 다음과 같다.
전체 반응식은 다음과 같다.[9]
:
그러나 이 반응은 탄산 칼슘이 물에 잘 녹지 않기 때문에 직접적으로 일어나지 않는다.[22] 솔베이 공정은 여러 단계를 거쳐 이 반응을 간접적으로 구현한다.
이 공정의 주요 폐기물은 염화 암모늄을 암모니아로 회수할 때 발생하는 염화 칼슘 용액뿐이다. 폐기물이 적다는 점은 솔베이 공정의 특징 중 하나이다.[22] 나트륨 기준 산업적 수율은 약 70%인데, 이는 중간 생성물인 중탄산나트륨이 물에 일부 용해되기 때문이다.[24]
1930년대 중국 화학자 후 더방은 염화 칼슘 대신 염화 암모늄을 부산물로 얻는 개선된 솔베이 공정을 개발했다. 이 공정을 통해 염화암모늄을 비료로 사용할 수 있어 폐기물 매립량을 줄일 수 있다.
3. 1. 탄산화 공정
포화 식염수에 암모니아와 이산화 탄소를 반응시켜 중탄산나트륨을 침전시킨다. 이 과정은 다음 화학 반응식으로 나타낼 수 있다.[22]:
이때 생성된 염화 암모늄은 이후 암모니아 증류 공정에서 수산화 칼슘과 반응하여 암모니아로 재회수된다.[22]
3. 2. 소성 공정
침전된 탄산수소 나트륨을 160~230°C로 가열(소성)하면 열분해되어 탄산 나트륨이 된다. 이 과정에서 이산화 탄소와 물이 부산물로 생성된다.[11]:
이때 발생한 이산화탄소는 탄산화 공정에서 재사용하기 위해 회수된다.[11] 즉, 이산화탄소는 일부가 재활용된다.[22]
3. 3. 암모니아 증류 공정
솔베이 공정에서 암모니아는 회수되어 재사용된다. 이 과정은 다음과 같다.[22]먼저, 석회석을 코크스와 함께 가열하여 산화 칼슘(생석회)과 이산화 탄소를 생성한다.
::
::
생성된 산화칼슘(CaO)은 물과 반응하여 수산화 칼슘(소석회)이 된다.
::
이 수산화칼슘은 염화 암모늄(NH₄Cl)과 반응하여 암모니아를 회수한다.
::
회수된 암모니아는 탄산화 공정에 재사용된다.[22] 이론적으로 암모니아는 모두 회수되어 소모되지 않는다.
4. 환경 문제 및 개선 노력
솔베이 공정은 탄산 나트륨 생산 과정에서 여러 환경 문제를 야기한다. 주요 부산물인 염화칼슘(CaCl₂)은 수용액 상태로 배출되며,[11] 공정 과정에서 발생하는 다른 폐기물과 함께 매립되거나 해양에 배출된다.
내륙 공장에서는 폐기물을 "폐기장"에 매립하는데, 이로 인해 토양 및 수질 오염이 발생한다. 뉴욕 솔베이의 폐기장은 인근 오논다가 호의 염도를 높여 심각한 오염을 유발했다.[13] 해안 지역에서는 염화칼슘 용액을 바다에 직접 배출하기도 하는데, 이는 해양 생태계에 영향을 줄 수 있다.[17] 특히, 인도 구자라트 주 사우라슈트라 지역의 배출 지역은 해양 국립공원 내에 위치하여 산호초, 해초 등에 피해를 줄 우려가 있다. 오스트레일리아 오스본에서는 침전지를 사용하여 염화칼슘을 제거하고 있으며,[17] 이탈리아 로지냐노 솔베이에서는 석회석 폐기물로 인해 "스피아제 비앙케"("흰 해변")가 형성되었는데, 이곳은 유엔환경계획(UNEP)에 의해 지중해 연안 오염 지역으로 등재되었다.[19]
탄소 격리를 위해 솔베이 공정을 변형하여 이산화탄소 배출을 줄이려는 시도도 있다.[20][21] 이산화탄소를 반응시켜 중탄산나트륨과 같은 고체 탄산염을 형성하여 영구 저장하는 방식이다. 그러나 이러한 방식은 추가적인 에너지 소비를 필요로 하며, 탄소 중립 에너지원을 사용하지 않으면 오히려 이산화탄소 배출량을 늘릴 수 있다.
1930년대 중국의 화학자 후더방은 염화칼슘 대신 비료로 사용 가능한 염화암모늄(NH₄Cl)을 부산물로 얻는 개선된 솔베이 공정(후더방 공정)을 개발했다.[11] 이 공정은 염화칼슘 생산을 제거하여 폐기물 매립량을 줄일 수 있다.[11]
4. 1. 염화칼슘 폐기물
솔베이 공정의 주요 부산물은 수용액 상태의 염화칼슘(CaCl₂)이다.[11] 이 공정에서는 다른 폐기물과 부산물도 발생한다. 소성되는 석회석 전부가 생석회(산화 칼슘)와 이산화 탄소로 전환되는 것은 아니다(반응 II). 잔류 탄산 칼슘과 석회석의 다른 성분들은 폐기물이 된다. 또한, 이 공정에 사용되는 염수는 마그네슘과 칼슘 이온을 제거하기 위해 정제되는데, 일반적으로 탄산염(탄산마그네슘(MgCO₃), 탄산칼슘(CaCO₃)) 형태로 제거한다. 그렇지 않으면 이러한 불순물이 반응 용기와 탑에 스케일을 형성하기 때문이다. 이러한 탄산염도 추가적인 폐기물이다.뉴욕 솔베이와 같은 내륙 공장에서는 부산물을 "폐기장"에 매립해 왔다. 폐기장에 매립된 물질의 무게는 생산된 소다회 무게보다 약 50% 더 많았다. 이러한 폐기장은 주로 칼슘과 염화물에 의한 수질 오염을 야기했다. 뉴욕 솔베이의 폐기장은 인근 오논다가 호의 염도를 상당히 증가시켰는데, 이 호수는 과거 미국에서 가장 오염된 호수 중 하나였으며,[13] 초유해 지역(superfund) 오염 지역이다.[14] 폐기장이 오래될수록 식물 군집을 지탱하기 시작하는데, 이는 여러 과학 연구의 주제가 되어 왔다.[15][16]
인도 구자라트 주 사우라슈트라 지역과 같은 해안 지역[17]에서는 CaCl₂ 용액을 바다에 직접 배출할 수 있는데, 상당한 환경적 피해 없이 가능한 것으로 보인다(소량의 중금속이 문제가 될 수 있지만). 주요 우려 사항은 배출 지역이 산호초, 해초 및 해조류 군집의 서식지인 쿠치만(Gulf of Kutch) 해양 국립공원 내에 위치한다는 것이다. 오스트레일리아 오스본에서는 이전 배출이 운하를 매립했기 때문에 현재 침전지를 사용하여 CaCl₂의 99%를 제거하고 있다. 이탈리아 토스카나 주 로지냐노 솔베이에서는 솔베이 공장에서 생산된 석회석 폐기물이 경관을 변화시켜 "스피아제 비앙케"(Spiagge Bianche, "흰 해변")를 만들었다. 1999년 유엔환경계획(UNEP)이 발표한 보고서에는 스피아제 비앙케가 지중해 연안 지역의 우선 오염 지역 중 하나로 등재되어 있다.[19]
4. 2. 이산화탄소 배출
솔베이 공정의 변형은 탄소 격리를 위해 제안되었다. 한 가지 아이디어는 석탄 연소 등으로 생성된 이산화탄소를 반응시켜 고체 탄산염(예: 중탄산나트륨)을 형성하고 이를 영구적으로 저장하여 대기 중으로의 이산화탄소 배출을 방지하는 것이다.[20][21] 솔베이 공정을 수정하면 다음과 같은 전체 반응식을 얻을 수 있다.: 2 NaCl + CaCO3 + CO2 + H2O → 2NaHCO3 + CaCl2
솔베이 공정의 변형은 이산화탄소 배출을 탄산나트륨으로 전환하는 데 제안되었지만, 탄산칼슘 또는 탄산마그네슘을 이용한 탄소 격리가 더 유망해 보인다. 그러나 칼슘이나 마그네슘을 이용하여 탄소 격리에 사용할 수 있는 이산화탄소의 양(인류가 배출하는 이산화탄소 총량과 비교했을 때)은 매우 적다. 이는 주로 석탄화력발전소와 같은 제어되고 농축된 배출원으로부터 이산화탄소를 포집하는 것과 소규모의 농축되지 않은 탄소원(예: 작은 불, 자동차 배기가스, 인간의 호흡 등)으로부터 탄소를 포집하는 것 사이의 실현 가능성에 큰 차이가 있기 때문이다. 게다가, 솔베이 공정의 변형은 대부분 추가적인 에너지 소비 단계를 추가할 것이며, 탄소 중립 에너지원(예: 수력 발전, 원자력 에너지, 풍력 또는 태양열 발전)을 사용하지 않는 한 이산화탄소 배출량을 증가시킬 것이다.
4. 3. 개선된 솔베이 공정 (후더방 공정)
1930년대 중국의 화학자 후더방은 기존 솔베이 공정을 개선하여 염화칼슘(CaCl₂) 대신 염화암모늄(NH₄Cl)을 부산물로 얻는 새로운 공정을 개발했다. 이 개선된 공정에서는 처음 몇 단계는 솔베이 공정과 동일하지만, 잔여 용액을 석회로 처리하는 대신 이산화탄소와 암모니아를 용액에 주입하고, 염화나트륨을 첨가하여 용액을 40°C에서 포화시킨다. 그 후 용액을 10°C로 냉각하면 염화암모늄이 침전되어 여과를 통해 제거되고, 남은 용액은 다시 탄산나트륨 생산에 사용된다.[11]후더방의 공정은 염화칼슘 생산을 제거하고, 대신 비료로 사용 가능한 염화암모늄을 생산한다. 염화암모늄은 염화칼슘보다 상업적 가치가 더 크기 때문에 폐기물 매립량을 줄일 수 있다는 장점이 있다.[11]
참조
[1]
논문
Solvay process
https://www.oxfordre[...]
Oxford University Press
2020-10-08
[2]
간행물
Soda Ash
http://minerals.usgs[...]
United States Geological Survey
2006
[3]
문서
The barilla used for soda ash production refers to any of several bushy plants that are well adapted to grow in salt marshes, and that are common in Spain and Italy. The ashes of these plants can contain as much as 30% sodium carbonate. The principal species for soda ash production were the "saltworts" Salsola soda or Salsola kali, but several other species could also be used.
[4]
논문
From the barrilla to the Solvay factory in Torrelavega: The Manufacture of Saltwort in Spain
https://web.archive.[...]
1998
[5]
서적
A Modern Herbal
http://www.botanical[...]
1931
[6]
논문
The Scottish kelp industry and its archaeology
http://www.lahsoc.or[...]
2012
[7]
논문
It was all about alkali
http://pubs.acs.org/[...]
2002
[8]
논문
Salts, Acids & Alkalis in the 19th Century. A Comparison between Advances in France, England & Germany
1951-12
[9]
논문
Soda Ash, Solvay Style
http://pubs.acs.org/[...]
2002-02
[10]
서적
Chemical Process and Design Handbook
McGraw Hill
2001
[11]
간행물
Process Best Practices Reference Document (BREF) for Soda Ash
https://web.archive.[...]
European Soda Ash Producer's Association
2004-03
[12]
서적
Chemistry Made Simple
https://archive.org/[...]
Broadway Books
2005
[13]
웹사이트
Onondaga Lake Partnership
http://www.onlakepar[...]
2006-10-14
[14]
웹사이트
superfund ID NYD986913580
http://cfpub.epa.gov[...]
U.S. Environmental Protection Agency
2006-10-14
[15]
논문
The flora and vegetation of an old Solvay process tip in Jaworzno (Upper Silesia, Poland)
2001
[16]
논문
Pedogenesis and invertebrate microcommunity succession in immature soils originating from chlor-alkali wastes
State University of New York College of Environmental Science and Forestry
1991
[17]
간행물
Technology in the Indian Soda Ash Industry
http://dsir.nic.in/r[...]
Department of Scientific and Industrial Research, Ministry of Science & Technology, India
1995-10
[18]
웹사이트
Penrice Soda Holdings Limited
https://archive.toda[...]
2006-10-14
[19]
논문
Identification of priority pollution hot spots and sensitive areas in the Mediterranean
http://wedocs.unep.o[...]
2020-09-11
[20]
간행물
Carbon dioxide sequestration by mineral carbonation: Literature Review
https://web.archive.[...]
Energy Research Centre of the Netherlands
2006-10-14
[21]
논문
Carbonate Chemistry for Sequestering Fossil Carbon
2002
[22]
서적
化学大辞典
共立
1981-10
[23]
웹사이트
戦間期東アジアにおける化学工業の勃興
https://web.iss.u-to[...]
2023-02-10
[24]
문서
[[#足立岩倉馬場2004|足立、岩倉、馬場 (2004)]] 28頁。
[25]
문서
[[#足立岩倉馬場2004|足立、岩倉、馬場 (2004)]] 26頁。
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com